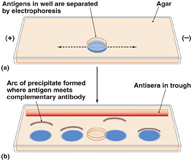
Como se puede observar en esta imagen, la técnica tiene dos fases bien definidas:
- Electroforesis, para separar los componentes antigénicos de la muestra que se ha depositado en el pocillo central. El pH del gel se selecciona de forma que las proteínas con carga negativa migren al ánodo o polo positivo. En el caso de muestras séricas, las proteínas suelen separarse en cinco regiones, ordenadas desde el ánodo al cátodo o polo negativo de la siguiente manera: Albúmina, alfa-1-globulinas, alfa-2-globulinas, beta-globulinas y gamma-globulinas. Las gamma-globulinas, por un fenómeno de electroendósmosis , migran hacia el cátodo.
- Doble inmunodifusión de las proteínas separadas previamente por la electroforesis y del antisuero situado en el surco, en el caso anterior el antisuero tendría anti- albumina, anti- alfa2globulina, anti beta globulina ademas de anti- IgG., anti-IgM y anti-IgA, y se colocaría lateralmente al recorrido electroforético.
Las bandas de precipitación tienen forma de arco, y se pueden teñir y comparar con las de un suero estándar o con el antígeno que se quiera identificar en la muestra.
En la imagen puedes ver una inmunoelectroforesis correspondiente a un caso de mieloma múltiple, una IgG con cadenas kappa. La técnica permite caracterizar la paraproteína gracias a los arcos de inmunoprecipitación formados contra antisueros específicos de cadenas pesadas y cadenas ligeras.
A la derecha de la inmunoelectroforesis se indican los antisueros utilizados. Para cada antisuero, en la parte superior se analiza una muestra del mismo paciente y, en la parte inferior, un suero control (NHS).
Se señalan los engrosamientos localizados en los arcos de precipitación correspondientes a los antisueros anti-IgG y anti-kappa. Esta intensa reacción anormal con anti-IgG y anti-kappa, y la falta de reacción con el antisuero contra las cadenas lambda, indican la presencia de una paraproteína monoclonal (IgG con cadenas kappa) ya que una inmunoglobulina policlonal reaccionaría con los dos tipos de antisueros anti-cadenas ligeras (anti-kappa y anti-lambda). La ausencia de una banda para anti-IgM y la presencia de una banda reducida para anti-IgA demuestran la típica reducción de inmunoglobulinas normales en esta enfermedad.
Entre las aplicaciones más importantes de la inmunoelectroforesis cabe destacar la caracterización de alteraciones cualitativas de proteínas específicas, por ejemplo, tal como se ha visto en un caso anterior, inmunoglobulinas monoclonales en mielomas, y el análisis de mezclas complejas de proteínas en fluidos biológicos.
La electroendosmosis en electroforesis se refiere al flujo de agua bajo la influencia de un campo eléctrico debido a grupos de carga inmovilizados en la matriz, principalmente grupos sulfato y carboxilo.
proliferación anómala de células plasmáticas malignas que producen en exceso una de las cadenas pesadas( de las moléculas de Ig (γ, α, µ ; G, A o M) y en exceso un tipo cadena ligera (κ, λ) (paraproteínas)
Se trata de una de las dos clases de cadenas ligeras que presentan las Inmunoglobulinas.
La proliferación monoclonal de las células plasmáticas dando como resultado una inmunoglobulina monoclonal o paraproteína, solo estarán presente una de las dos cadenas ligeras de las Inmunoglobulinas( Kappa o Lamda).
Se trata de una de las dos clases de cadenas ligeras que presentan las Inmunoglobulinas
Se trata un único tipo de cadena ligera y/o pesada (componente monoclonal) que cuando está en exceso produce algún tipo de gammapatía.
Cuando la inmunoglobulina presenta tanto cadenas ligeras kappa o lambda
Coeficiente que indica el grado de acidez o basicidad de una solución acuosa.