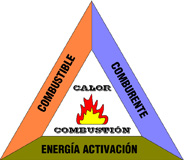
Piensa en algo que pueda quemarse. ¿Qué reacciones químicas crees que caracterizan la combustión?
Todos los combustibles tienen como base dos elementos químicos, el Carbono (C) y el Hidrógeno (H), y para que se produzca la combustión es necesario que existan además un comburente que es el Oxígeno (O) y una energía de activación que se encarga de iniciar la reacción química.
Además los combustibles suelen contener otros elementos químicos como puede ser el Azufre (S). El Oxígeno (O) necesario se obtiene del aire, que mayoritariamente contiene Nitrógeno (N).
Con todos estos elementos se activan varias reacciones químicas exotérmicas que debes conocer:
| Reacción Carbono | Reacción Hidrógeno | Reacción Azufre | Reacción Nitrógeno |
|---|---|---|---|
Tanto el SO2 como los NOx son importantes porque combinados con el Agua (H2O) producen respectivamente Acido Sulfúrico y Acidos Nitrosos, estos últimos son los culpables de la lluvia ácida.
Si observas las reacciones anteriores puedes ver que se necesita un número exacto de unidades de cada uno de los elementos químicos involucrados, cuando esto ocurre tenemos la combustión estequiométrica, pero en la realidad la combustión se realiza con defecto o exceso de alguno de los elementos.
La combustión reductora se lleva a cabo con defecto de oxigeno y tiene inconvenientes por producir:
- Monóxido de Carbono (CO) que es tóxico y puede ser mortal en ciertas concentraciones para los seres vivos.
- Inquemados que son restos de combustible que crean capas de suciedad.
La combustión oxidante es la más adecuada y se realiza con exceso de oxígeno, por lo que también se denomina combustión completa. El índice de exceso de aire recomendable depende del tipo de combustible utilizado.
Sustancia que participa en la combustión oxidando al combustible, tratándose normalmente del oxígeno del aire.
Es la energía necesaria para iniciar una reacción química, en este caso la de combustión.
Proceso en el que se desprende energía.
Son las precipitaciones en las que vienen mezcladas óxidos de nitrógeno y dióxido de azufre en forma de ácidos, por lo que producen importantes deterioros en el ambiente.
Reacción química en la que la proporción de reactivos es exacta por lo que la reacción es completa.
Reacción química en la que existe defecto de oxígeno por lo que la reacción es incompleta.
Reacción química en la que existe exceso de oxígeno por lo que la reacción es incompleta.
Es la relación entre el aire realmente utilizado en la combustión y el aire estequiométrico que le corresponde a un determinado combustible.